 Sivuston teko on kesken | ||||||||||||||||
|
Pääsivu
Alkusivu
Sivujen tekijä
Oscaristit
Sivukartta
Ohjeita
Mattosuodatin
Kypsytys
Akvaario
Kalat
Kasvit
Ravut/äyriäiset
Taudit
Tutkiminen
Lääkitys
Yleisohjeet
Lääkevalmisteet
Lääkeaineet
Itse tehdyt
Tanganjika
Tanganjika-järvi
Tanganjika-akva
Aloittelijoille
|
Pääsivu - Sivukartta - Akvaario - Akvaariolinkkini M. Veteen liuonneet mineraalit, hapot ja emäkset sekä niiden merkitys
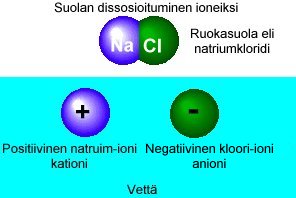
Ionit Vesi on erinomaisen hyvä liuotin. Lähes kaikki aineet liukenevat ainakin jossain määrin. Jotkut aineet liukenevat kokonaan lisäyksestä riippumatta, mutta toisilla on tietty liukoisuuden yläraja. Kun tämä yläraja on saavutettu sanotaan veden olevan kyllästynyt kyseisellä aineella. Toiset aineet liukenevat erittäin nopeasti ja jopa välittömästi. Liukeneminen voi olla niin kiivasta, että siitä syntyy lämpöä! Näin käy jos esimerkiksi rikkihappoa lisätään veteen (erittäin vaarallista). Kun happoa ja emästä sekoitetaan keskenään, saadaan suolaa; niinpä kun Natriumlipeää (NaOH) ja suolahappoa (HCl eli kloorivetyä) sekoitetaan, saadaan natriumkloridia eli tavallista ruokasuolaa (NaCl) ja vettä (H2O). Reaktio on seuraava: natriunhydroksidi + kloorivety = natriumkloridi + vesi Suoloilla on kemiallinen nimi aina sen mukaan minkä hapon ja emäksen suolasta on kysymys:

IonitKun happoa, emästä tai jotain suolaa liuotetaan veteen, niin aine hajoaa joko kokonaan tai osittain ioneiksi.
Ionit ovat aineen osasia, joko atomeja tai atomiryhmiä (molekyylejä), jotka ovat menettäneet tai saaneet elektroneja.
Elektroni on negatiivisesti varautunut hiukkanen atomissa. Ionit ovat sähköisesti varautuneita ja ne antavat vedelle
tiettyjä ominaisuuksia. Esimerkiksi natriumkloridi eli tavallinen ruokasuola hajoaa veteen liuenneena kokonaan
Na+- ja Cl-- ioneiksi. Ionien sähköistä varausta kuvataan
joko + tai - merkillä.
Reaktiossa natrium menettää elektronin ja saa siten positiivisen varauksen (Atomin ytimessä on nyt yksi positiivinen protoni elektroneja enemmän.). Vastaavasti kloori saa yhden elektronin lisää, ja siten negatiivisen varauksen. Negatiivisesti varautuneita ioneja kutsutaan anioneiksi, ja positiivisesti varautuneita kationeiksi. Eri atomeilla ja molekyyleillä on joko yksi tai useamman arvoisia ioneja sen mukaan montako elektronia se dissosiaatiossa joko luovuttaa tai vastaanottaa. Natrium luovuttaa yhden elektrodin, mutta kalsium luovuttaa kaksi. Vastaavasti kloori ottaa yhden elektronin, mutta esimerkiksi sulfaatti ottaa kaksi.

Vahvat hapot ja emäkset sekä niiden suolatVahvat hapot-, emäkset ja niiden suolat dissosioituvat kokonaan. Vahva happo tai emäs tunkeutuu heikon hapon tai emäksen tilalle ko. suolaan, jolloin heikko happo tai emäs vapautuu. Tähän reaktioon perustuu esimerkiksi kalkkikiven "kuohuminen" kun sille tiputetaan suolahappoa. Tällöin kalsiumbarbonaatista muodostuu kalsiumklodidia ja hiilihappo (hiilidioksidi) kuplii ilmaan. 
Heikot hapot ja emäkset sekä niiden suolatHeikot hapot, emäkset ja niiden suolat dissosioituvat vain osittain. Niinpä vedessä on samanaikaisesti sekä hiilihappoa että hiilidioksidia. Ammoniakki on heikko emäs ja esiintyy vedessä sekä vapaana ammoniakkina että ammoniumhydroksidina. Ammoniakki on voimakas myrkky kaloille. Happamessa ympäristössä kaikki ammoniakki sitoutuu happoihin, jolloin muodostuu happoja vastaavia ammoniumsuoloja. 
Suola- eli mineraalipitoisuusSuolapitoisuus kuvaa kaikkien veteen liuenneiden suolojen kokonaismäärää. Suolapitosuus vaikuttaa osaltaan myös veden osmoottiseen paineeseen. 
Sähkönjohtokyky eli johtavuusIonit pystyvät kuljettamaan sähköä. Mitä enemmän vedessä on ioneja, sitä paremmin vesi johtaa sähköä. Veden sähkönjohtokyky voidaan mitata. Saatu tulos kuvastaa vedessä olevien ionien kokonaismäärää eli suolapitoisuutta.
|
|||||||||||||||
 Suuri johtokyky
Suuri johtokyky